A humán mikrobiom hatása ma már megkérdőjelezhetetlen, és az intenzív kutatások eredményeképpen egyre több információnk van ezen a területen. A tápcsatornában megtelepedő baktériumok és különösen a bélflóra megismerésére, összetett hatásainak feltérképezésére óriási erőforrásokat összpontosítanak az utóbbi években. Mivel az egészségipar és az élelmiszeripar területén is jelentős perspektívát látnak a mikroorganizmusok szerepének kiaknázásában, az ez irányú kutatások még nagyobb lendületet kaptak.
Mint ahogyan az Élet és Tudomány 2015/12. számában megjelent cikkben több esetben is láthattuk, a mikroorganizmusok nem válnak szét jó és rossz baktériumokra, aktuális szerepük sok tényezőtől függ. Az egészséges állapot egy egyensúlyi helyzet, amely különböző módon kialakulhat és fenntartható, nincs hozzá egy kulcs, mint ahogyan nincsenek mindenre ható csodaszerek sem. Ennek ellenére fontos terápiás célpontok lehetnek a bennünk élő mikrobák, de ezek precíz alkalmazásához sokat kell még tanulnunk.
A szájunk Kánaán
A tápcsatorna kezdete nem a legkönnyebb terep a baktériumok számára, hiszen a nyál többféle antibakteriális anyagot termel, a szájüregben egyebek között a sejtfalszintézist gátló lizozim és a laktoperoxidáz nevű enzim is gátolja a baktériumok szaporodását. Ennek ellenére a több embert párhuzamosan vizsgáló kutatások során összesen több mint 600 fajt azonosítottak a szájüregben (Actinomyces-, Bacteroidetes-, Capnocytophaga-, Lachnospiraceae-, Lactobacillus-, Leptotrichia-, Neisseria-, Prevotella-, Selenomonas-, Streptococcus- és Treponema-fajokat). Természetesen ezek nem mindegyike található meg mindenkinél, és a csoportok egymáshoz viszonyított arányai is változhatnak.
A mikroba-Kánaán a fogak és az íny felszínén van, ahol különleges biofilm képződhet oxigénlimitált (anaerob közeli) környezetet kialakítva. Itt nagyobb lehet a tápanyagok koncentrációja és dentális plakknak nevezett lerakódás alakulhat ki, amely még frissen mosott fogaknál is felfedezhető. Ehhez a nyálból származó glikoproteinek képezik az alapot, amelybe különböző Streptococcusok fészkelik be magukat, majd őket más csoportok (például Fusobacterium, Borrelia és Actinomyces) képviselői követik, melyekkel közösen alakítják ki a fogromlást előidéző körülményeket. A két fő bűnös a Streptococcus sobrinus és a Streptococcus mutans, mindkettő savat termelő baktérium. A S. sobrinus nagy affinitással tapad ki a glikoprotein mátrixhoz, az S. mutans pedig szacharózból (a közönséges asztali cukorból) dextránt csinál, amellyel a fogak felszínéhez köt. Összetett közösség alkotja tehát a dentális plakkot, amely a jó oxigénellátottságú szájüregen belül kialakított anaerob mikrokörnyezet – a baktériumok itt saját maguknak ágyaznak meg, persze a mi hathatós közreműködésünkkel. A tápanyagot a baktériumok ugyanis az általunk elfogyasztott táplálékból szerzik. A plakkon belül a tejsavbaktériumokhoz tartozó számos Streptococcus-faj savas anyagcsereterméke oldja a fogak kalcium-foszfát-tartalmát, így azok szerkezete sérül, a baktériumok egyre mélyebben hatolnak a fogba, miközben enzimjeik a környező szöveteket is roncsolják.
Nem mindegy tehát, hogy mivel etetjük ezeket a fognyűvő manókat. A kutatások szerint azokban az országokban, ahol szinte nem fogyasztanak cukrot, ott nincs jelen a plakkban az S. mutans, és fogszuvasodás sem alakul ki. Európában és az USA-ban ellenben szinte mindenki találkozik a problémával és tudtán kívül az S. mutanssal is, hiszen ezeken a területeken a vizsgált személyek 80–90 százalékában kimutatható ez a baktérium. Nehéz persze változtatni régi szokásainkon, de érdemes ilyen szempontból is figyelnünk arra, hogy mit eszünk. Van persze más teendőnk is, hogy elkerüljük a fogszuvasodást: a plakk alapját képező glikoproteinek lemoshatók a fogról, és az ételmaradékok eltávolításával szintén érdemes megnehezítenünk a baktériumok dolgát.
Otthon, édes otthon
A gyomor fő funkciója a táplálék emésztése, de emellett fontos az is, hogy sok lenyelt baktériumot tesz ártalmatlanná. Az itt jellemző savas közeg, az emésztőenzimek és bizonyos antimikrobás anyagok nagyon barátságtalan hellyé teszik a gyomrot a legtöbb élőlény számára, ezért sokáig úgy gondolták, hogy itt egyáltalán nem alakul ki semmiféle baktériumközösség. Kevés hely van azonban a világon, ahol valamilyen baktérium ne tudna megtelepedni. Egyes fajok nemcsak hogy életben tudnak maradni extrémnek tartott körülmények között, de amelyek ilyen élőhelyeken élnek, azok általában igénylik is a számunkra elviselhetetlennek tűnő feltételeket.
1983-ban fedezték fel a Helicobacter pylori nevű fajt, amely azóta meglehetősen nagy ívű karriert futott be, hiszen nemcsak váratlan helyen bukkant fel, de számos betegséggel is összefüggésbe hozták. Rengeteg tanulmány készült, amelyben ennek a baktériumnak a szerepét próbálják tisztázni például a gyomorhurut, gyomorfekély vagy akár a gyomorrák kialakulásában. Ha figyelembe vesszük ugyanakkor, hogy a teljes népesség felében megtalálható, sőt domináns ez a mikroorganizmus, ismét felmerülhet a kérdés, hogy ez akkor beletartozik-e a „normális” kategóriába. Nehéz erre válaszolni, főleg hogy más kutatások szerint olyan betegségek, mint a nyelőcsői reflux, gyulladásos bélbetegség, gyermekkori asztma ritkábban alakulnak ki olyan személyeknél, ahol a H. pylori megtalálható.
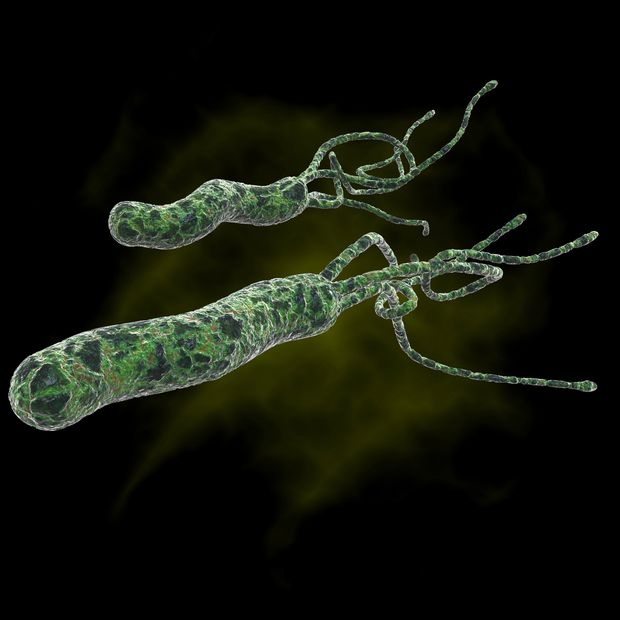
Mindenesetre attól a pillanattól, hogy a gyomrot már élhető habitatnak tartották, megindultak a kutatások más, itt élő baktériumok után is. Fontos lehet ebben az esetben az élő kitétel, mivel a kimutatási módszerekből adódóan van egy kis nehézsége a gyomor-
mikroflóra-vizsgálatoknak. A DNS-alapú módszerek ugyanis nem garantálják, hogy a gyomorban élő baktériumokat mutatjuk ki, és nem csak azoknak a baktériumoknak a lenyelt, majd megemésztett, de még ép és elemezhető DNS-molekuláit, amelyek soha nem is voltak életképesek itt. A tenyésztéses és DNS-technikákat is alkalmazó tanulmányok alapján a gyomornak jellegzetes baktériumközössége van, amely elkülönül a szájüreg és a nyelőcső mikroflórájától. Ebben a saját ökoszisztémában diverz társaság él, de nem túl nagy tömegben, a legjelentősebb nagy baktériumcsoportok a Proteobacteria (ide tartozik a Helicobacter pylori is), Firmicutes, Actinobacteria és a Bacteroidetes. Ha nemzetségek szintjén nézzük az összetételt, akkor a Helicobacteren kívül itt is megjelennek a Lactobacillusok (Firmicutes), Streptococcusok (Firmicutes), Staphylococcusok (Firmicutes), Propionibacteriumok (Actinobacteria), Bacteroidesek (Bacteroidetes). Az, hogy a Helicobacterium pylori jelenléte mennyire hat a közösségi összetételre, arról megoszlanak a vélemények, de inkább az az álláspont gyakoribb, hogy kevésbé. Ellenben csakúgy, mint más szervek vagy testrészek esetében, a gyomorban is nagy az egyének közötti változatosság.
Az utolsó kanyar
Az egész humán mikrobiom döntő hányada a bélrendszerben található, ez az összes baktériumsejt 90 százalékát jelenti, tehát körülbelül 1013–1014 egyedszámú baktériumot. Nem véletlen, hogy a legtöbb információnk az itt kialakult mikroflóráról van, hiszen mennyiségét, összetettségét és valószínűleg hatásait tekintve is a humán bélflóra kiemelkedik a többi, emberi testen kialakuló mikrobaközösség közül. Vizsgálatára külön projekt szerveződött, több európai kutatóintézet bevonásával. A MetaHIT- (Metagenomics of the Human Intestinal Tract) program – a teljes bélflórát vizsgálva – a bélbaktériumok és az egészséges, valamint a kóros állapotok közötti kapcsolatok feltárására jött létre, különös tekintettel a krónikus bélgyulladásra és az elhízásra, amelyek nemcsak Európában jelentenek egyre nagyobb problémát. A bélrendszer mikrobaösszetétele természetesen nem mutat egységes képet, hiszen teljesen más körülmények vannak például a vékonybél elején, mint a vastagbélben. Jellemzően a gyomortól távolodva a baktériumszám emelkedése mellett nő a pH, és csökken az oxigénszint. A vékonybél elején, a duodenumban még savas a pH, és itt a mikroflóra hasonlít a gyomoréhoz, a vékonybél vége felé a bélbaktériumok száma eléri a 105–107sejt/gramm béltartalom-értéket. Ezen a szakaszon már jellemzőek az anaerob baktériumok, amelyek kerülik az oxigénnel való találkozást, és ahogy átlépünk a vastagbélbe, már egy valódi fermentáló edénybe érkezünk, ahol a maradék oxigént fakultatív aerob baktériumok fogyasztják el. Ebben a szigorúan oxigénmentes környezetben az egyéb Gram-pozitív csoportok mellett megjelennek a Clostridium- és Bacteroides-fajok is. A bélflóra folyamatosan változik és megújul, naponta átlagosan 1013 darab baktériumsejt ürül a széklettel, amely tömegének akár harmadát is adhatja a bakteriális biomassza.
Az utóbbi években szinte mindennel összefüggésbe hozták a bélbaktériumokat, sok esetben azonban még nem tisztázott, hogy egyes élettani jelenségekre milyen mechanizmus alapján fejti ki hatását a bélflóra, és esetenként ellentmondásos kutatási eredmények is születtek. Az elhízás az egyik olyan összetett probléma, amelynek kapcsán a bélbaktériumok szerepe egyre inkább felvetődött az utóbbi időben, és nem azért, mert ezeknek a baktériumoknak a tömege összesen akár a 3 kilót is elérheti. Több kísérletben kimutatták, hogy az elhízott emberek mikrobiótája más, ami logikus, hiszen a belünkben élő baktériumok azt és annyit esznek, amit és amennyit mi. A baktériumok segítségével az elfogyasztott táplálékból hatékonyabb lehet az energiaszerzés (bár az elhízás szempontjából ez már nem feltétlenül előny), például az emészthetetlen rostok fermentálásával egyes bélbaktériumok elérhető tápanyagforrást termelnek nem csak a többi baktériumnak, de a bélfal sejtjeinek és a környező szöveteknek is, amely egyik tényezője lehet az elhízásnak. Egerek esetében sok bizonyíték van arra is, hogy a baktériumoktól teljesen mentesített egyedeknél nem lehet pusztán az étrenddel elhízást kialakítani, és esetükben több kalória ürül a bélsárral, valamint hogy az elhízás a bélflórával tulajdonképpen átültethető. Ember esetében ezekre az összefüggésekre egyelőre nincsenek közvetlen bizonyítékok, az azonban bizonyos, hogy az étrendünk befolyásolja a bélflórát, amely hat az anyagcserére.

Nemcsak az elhízás kapcsán merült fel ezeknek a mikroorganizmusoknak a szerepe, hanem számos más anyagcsere-betegség esetében is. Ilyen például a 2-es típusú cukorbetegség, de szív és érrendszeri problémák kialakulásában is közrejátszhatnak. Jelenlétükkel és anyagcseretermékeikkel befolyásolják az immunrendszert, sőt mi több, a bélmikrobióta tagjai idegrendszerünkre hatva a hangulatunkra is befolyással vannak.
A bélflórán belül kiemelt figyelem irányul az úgynevezett probiotikumokra, ezek olyan bélbaktériumok, amelyek pozitív hatással vannak az egészségünkre. Lactobacillus-fajok és a Bifidobacterium nemzetség tagjai kapták ezt a kitüntető címet, és az ezek bizonyos törzseit tartalmazó gyógyászati készítmények vagy élelmiszerek nagyon népszerűek mostanában, éppen azért, mert a kutatások bizonyították, hogy ezek a baktériumok jó hatással vannak az egészségünkre. Az azonban máig kérdéses, hogy ezeknek a termékeknek a fogyasztása képes-e helyreállítani az egészséges bélflórát. A kételyek ellenére több betegség kezelésében is kimutatták a probiotikumok fogyasztásának jótékony hatásait, bár ennek pontos mechanizmusát többnyire még keresik.
Mivel a velünk élő baktériumoknak ilyen szerteágazó és nagyon jelentős hatásuk van az egészségünkre, fontos, hogy ne romboljuk le ezt a jó együttműködést. Az antibiotikumok például többnyire nemcsak a kórokozókat, hanem a jótékony baktériumokat is megölik vagy gátolják, de fontos szerepe van az étkezésnek és más szokásainknak is a normál flóra fenntartásában. Tudjuk, hogy vannak számunkra ártalmas mikroszervezetek és olyanok, amelyek szerepe még kérdéses, és léteznek olyanok, amelyek bizonyítottan szükségesek egyes betegségek elkerüléséhez, egészségünk megőrzéséhez. A természet azonban nem szigorúan körbehatárolt kategóriákban létezik, így a normál flóra meghatározása is nehéz, hiszen a velünk élő baktériumközösségek folyamatosan változnak, és dinamikus kölcsönhatásban vannak testünkkel, valamint környezetünk más elemeivel. Ezeknek a baktériumoknak a teljesebb megismerése és szerepük pontos feltárása segíthet megőrizni vagy akár helyreállítani is az egészséges állapotot. Éljünk hát velük!
TÓTH ÁKOS
2015/14