Mengyelejev periódusos rendszerének 33-as rendszámú eleme kétes hírnévnek örvend. Az arzénről legtöbbünknek a mérgező anyag jut először eszébe, viszont az kevésbé köztudott, hogy régóta alkalmazzák gyógyszerként. Így jogosan tehetjük fel a kérdést, lényegében melyik táborba sorolhatjuk az iménti kémiai elemet és annak radioaktív izotópjait?

Magyarázatként a Paracelsus által megfogalmazott néhány mondat szolgál, amit a toxikológia őstanának tekintenek: Mi az, ami nem méreg? Minden anyag méreg, és nincs semmi méreg nélkül. Egyedül a dózis határozza meg, hogy mi nem mérgező. Ez magában foglalja a méregtan egyik legfontosabb alapfogalmát is, a dózist, amely koncentrációegységekben (például mg vagy ľg/testsúly kg) adja meg a mérgező anyag mennyiségét a szervezetre. Paracelsus tézisére jó példa az arzén, amit már kétezer évvel ezelőtt is használtak orvosságként a görögök és a kínaiak, de ugyanúgy kiérdemelte a mérgek királya, a királyok mérge jelzőt is, mivel évszázadokon át alkalmazták méregként a hatalomra éhes trónkövetelők vagy a férjüktől máshogy megszabadulni nem tudó asszonyok.
Méreg vagy gyógyszer?
Először Hippokratész alkalmazta gyógyszerként, aki már a Kr.e. 5. században is kezelt fekélybetegeket realgár (As4S4) és auripigment (As2S3) pasztákkal. Több ókori civilizáció is alkalmazta az arzént orvosságként, például a kínaiak sikeresen használták a fehér arzént (arzén-trioxid) a malária ellenszereként, és a perzsáknál is találunk említést a láz fehér arzénnal történő kezelésére.
A következő nagy áttörést a Paul Erlich által 1909-ben felfedezett Salvarsan nevű, szerves arzéntartalmú antibiotikum jelentette. Erlich arzénvegyületeket vizsgált, hogy képesek-e baktériumokat elpusztítani, és végül sikeresen alkalmazta a szert a szifilisz kórokozói, a spirochaeta-baktériumok ellen.
Az 1970-es években a kínai Harbin Egyetemen arzén-trioxidot nyomnyi mennyiségű higannyal együtt használva, eredményesen kezelték a leukémiát. Az arzént radiogyógyszerként jelenleg is alkalmazzák kísérleti fázisban, izotópjától, vagyis annak bomlási módjától függően mind a diagnosztikában, mind terápiás eljárásokban.
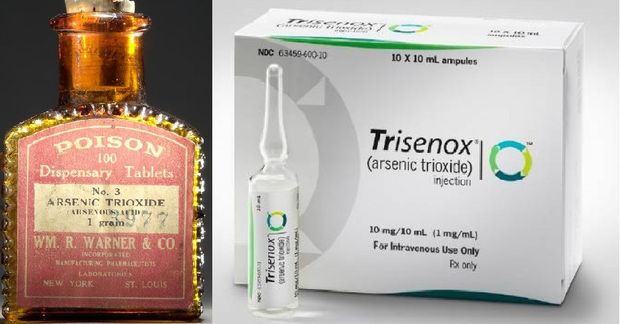
Arzén-trioxid – minden a dózistól függ
Az arzén sötétebbik oldalát valószínűleg mindenki jobban ismeri. Számos művészeti és történelmi említést találunk, ahol az arzén mérgező tulajdonságát használták fel. Először Flaubert Bovarynéját említhetjük, ahol a címadó főhősnő arzénnal követ el öngyilkosságot. Vagy ott vannak Agatha Christie, a világhírű írónő népszerű művei, Joseph Kesselring Arzén és levendula című krimikomédiájában idős testvérpár édesíti meg magányos férfiak utolsó óráit ribizliborba kevert arzénnal.
A nagyrévi sorozatgyilkosságok névvel elhíresült történet szerint a XX. század elején helybeli asszonyok élükön a település bábájával férfiak tucatjait tették el láb alól úgy, hogy arzént kevertek ételükbe, italukba.
Talán a legismertebb arzénmérgezés a történelem során Napóleon nevéhez fűződik. A történelemkönyvek szerint a halál oka gyomordaganat volt, ám hívei között erősen élt az az elképzelés, hogy a császárt az angolok ügynökei mérgezték meg. A neutronaktivációs analitikával elvégzett mérések nem bizonyították az arzénmérgezést, csak antimontartalmú gyógyszer szedését, ezt 1982-ben a Nature-ben publikálták is. A kételyt 2007-ben oldotta meg egy nemzetközi tudóscsoport, a történelmi tényeket és Napóleon alkoholban tartósított gyomrát egyaránt felhasználva. A vizsgálatok egyértelműen kimutatták, hogy az egykori császár halálát gyomorrák okozta.
Radioaktivitás a gyógyászatban
A radioaktivitás legfontosabb alkalmazása a természettudományokhoz köthető, azon belül az orvosbiológiai kutatásokhoz. Ennek alapkövét Hevesy György fektette le a radioaktív izotópon alapuló nyomjelzéses technika kidolgozásával. A radioaktív izotóp detektálásával a szervezetben nyomon követhető, hogy milyen utat jár végig a jelzett molekula, és arra is következtethetünk, hogy a biokémiai folyamatok során milyen molekulákba juthat át eközben. Az orvosi alkalmazás alapelve, hogy a biológiai rendszerek (például az emberi szervezet) az egyes elemek izotópjai között nem tesznek különbséget, vagyis ugyanazon kémiai elem inaktív, illetve radioaktív izotópja ugyanúgy viselkedik, ugyanazt az utat járja be a szervezetben. Munkásságának elismeréseként Hevesy, radioaktív izotópok indikátorként való alkalmazásáért a kémiai kutatásban indoklással 1943-ban Nobel-díjat kapott. A módszer alkalmazásával a kutatók, orvosok olyan vizsgálati lehetőséghez jutottak, amilyenről korábban nem is álmodhattak.

Ciklotron és oktatóreaktor, valamint a velük előállítható izotópok
Az arzén egyetlen stabil izotópja a 75-ös tömegszámú, a többi radioaktív. A radio jelentése sugárzás, a radioaktív izotópok sugárzással adják le energiafeleslegüket, hogy stabil izotóppá váljanak. Az arzénizotópok két nagy csoportra oszthatók, a negatív béta-bomló izotópokra, amik elektront (e-) adnak le, illetve a pozitív béta-bomlókra, amik az elektron antirészecskéjét, a pozitront (e+) adják le. A sugárzásuk alapján lehet a felhasználásukat csoportosítani: a pozitív béta-bomló izotópokat a diagnosztikában alkalmazzák, amikor felderítik, keresik a betegségeket, a negatív béta-bomló izotópot tartalmazó radiogyógyszereket pedig a terápia, vagyis a betegségek kezelése során alkalmazzák.
Izotópdiagnosztika esetén az élő emberi szervezetbe olyan radioaktív készítményeket juttatnak be, amelyek részt vesznek a fiziológiai, biokémiai folyamatokban, de anélkül, hogy azok végbemenetelét befolyásolnák. Terápiás alkalmazás esetén viszont az a cél, hogy az izotóppal jelölt biomolekula a kóros szövetekben dúsuljon fel. Így az izotóp által kibocsátott sugárzás végzi a célzott sejtpusztítást, ami tulajdonképpen az elemi részecskék dimenziójában lezajló sebészeti beavatkozás.
Orvosbiológiai felhasználás
A pozitív béta-bomló izotópokat tartalmazó radiogyógyszerek fő alkalmazási területe a Pozitron Emissziós Tomográfia (PET), ami egy sebészeti beavatkozást nem igénylő diagnosztikus eljárás. A bomlás közben pozitront kibocsátó izotópok előállítása ciklotronnal történik. Ez egy részecskegyorsító, ahol a mágneses térnek köszönhetően a részecskék belülről kifelé haladnak a spirális térben. Ezekkel a részecskékkel ütköztetve a céltárgyat, létrehozhatjuk a kívánt radioaktív izotópokat. Arzén esetében természetes germánium céltárgyat használnak, amiből közvetlenül arzénizotóp keletkezik. Az arzénizotópok közül a 71, 72 és a 74-es tömegszámú izotópok pozitron-bomlók, tehát PET-eljárásoknál jól használhatók.
A negatív béta-bomló izotópokkal jelölt gyógyszermolekulákat elsősorban terápiás célokra alkalmazzák, illetve speciális képalkotó diagnosztikákban. Előállításuk reaktorral történik, ami ebben az esetben nagy neutronforrásként szolgál, és a neutronok aktiválják radioaktívvá a besugárzott anyagot. Arzén esetében a célanyag természetes összetételű germánium-dioxid, ami először radioaktív germániummá aktiválódik, és később ez bomlik tovább radioaktív arzénná. A reaktoros besugárzás esetén nemcsak radioaktív arzént nyerünk, hanem radioaktív germániumot is fog tartalmazni az aktivált minta. Éppen ezért használják az arzén 77-es izotópját radiokémiai elválasztási módszerek optimalizálására, mert az elválasztási folyamat fejlesztése során mindkét izotóp nyomon követhető nukleáris méréstechnikai módszerekkel. Nukleáris mérések során akár egyetlen atom is detektálható, ami a kémiában ismert molalitás (6,022×1023 db atomot jelent egy mól) töredékrésze, így érzékeny analitikai eljárások kifejlesztése vált lehetővé.
Megfelelő kémiai elválasztási módszer alkalmazása után a radioaktív arzénizotóp elválasztható a besugárzott germánium-dioxid targettől, és tiszta arzénfrakció nyerhető, ami megfelelő potenciál a radiogyógyszer gyártásban.
Új eredmények
Az új radiogyógyszerek tervezésénél nehéz a radioaktív nyomjelzőt úgy hozzákötni a molekulához, hogy ne történjen jelentős szerkezeti változás. Épp ezért, ha arzénizotóppal akarjuk jelölni a biomolekulát, az egyik lehetséges megoldás, ha a nitrogént vagy a foszforatomot cseréljük le arzénra, mivel mindhárom elem a periódusos rendszer ugyanazon oszlopába tartozik, így kémiailag hasonlók. Ráadásul mindkét elem (nitrogén, foszfor) gyakori a biológiailag aktív molekulákban. Erre példa a kolin bioszintézise, amikor nitrogént cseréltek ki arzén-72 izotópra, a jelzett vegyületet pedig PET-diagnosztikumként alkalmazták állatkísérletekben.
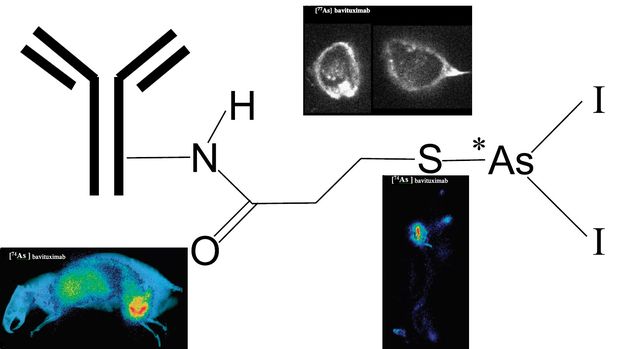
Bavituximab kísérleti fázisú diagnosztikus és terápiás alkalmazása
Másik lehetséges jelölési módszer, ha az arzénizotópot egy kéntartalmú biomolekulához kötjük, mert az arzén a kénnel erős kovalens kötést hoz létre. Utóbbira példa az As-74 jelölése egy bavituximab nevű speciális fehérjével. Ez a fehérje egy antitest (ellenanyag), ami a tumorok felületén található zsírokhoz kötődik. A fehérjéhez egy speciális, kéntartalmú oldalláncot kötnek hozzá, ami erős kovalens kötéssel kapcsolódik az arzénhoz. Ebben a technikában az alkalmazott arzén mennyisége milliomod része a mérgező szintnek, és kisebb aktivitású, mint az általában alkalmazott izotópok.
Az arzén-77 izotóp teljes mértékben negatív béta-bomló, ami lehetővé teszi terápiás radiogyógyszerként való alkalmazását, az intravaszkuláris sugárterápiában (éren belüli besugárzás), továbbá a radioimmunoterápiában (immunsejtekhez kötik az izotópot), ami a rossz irányú folyamatokat például autoimmun betegségek esetén visszafordíthatja a megfelelő irányba. Szinovektómiás alkalmazása is ismert, amikor az ízületi folyadék túltermelését kell megakadályozni. Az előbb említett bavituximab nevű fehérje is ígéretes molekula, ha arzén-77 izotóppal jelöljük arzén-74 helyett, akkor szintén alkalmassá válik terápiás alkalmazásra.
Egy új alkalmazási területe az orvosi izotópoknak a teranosztikus felhasználás. Ebben az esetben a diagnosztikus és terápiás tulajdonságokat egyetlen ágensben kombinálják, illetve egyénre szabott terápiákat lehet kialakítani számos betegség esetén. Erre példa az As-72 izotóp, ami többféle sugárzással adja le többletenergiáját, ezért alkalmas egyszerre diagnosztikus és terápiás alkalmazásra. Az eddigi vizsgálatokban ezt az izotópot egy TRC105 nevű antitesthez kötötték, ami kénatomot tartalmaz, így az arzén direkt hozzáköthető. A TRC105 egy olyan transzmembrán fehérjéhez kötődik, ami vérerek növekedésének és működésének fenntartásában vesz részt, így az érből kiinduló rákos sejtek szaporodását csökkenti.
Az említett molekulák még nem törzskönyvezett radiogyógyszerek, tehát humán felhasználásuk nem engedélyezett, de több olyan is akad köztük, ami már a gyógyszerfejlesztés utolsó állomásaiban van, és sikeres zárókísérletek után, pár év múlva radiogyógyszerként is használható lesz.
BALATONI- OLÁH ZITA
2016/29





