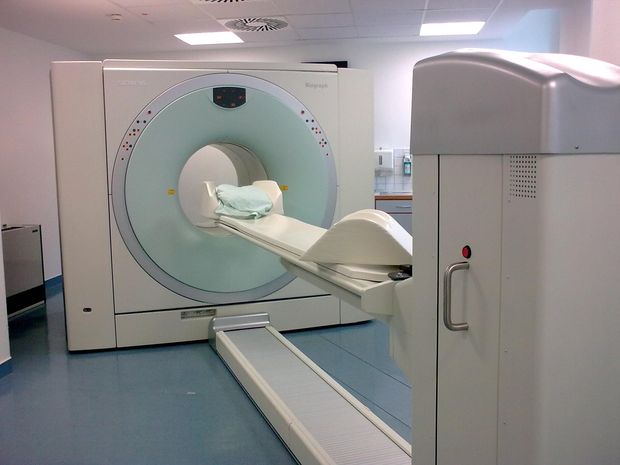
Napjainkban a komputertomográffal kombinált pozitronemissziós tomográfia (PET/CT) az egyik legmodernebb, sebészeti beavatkozást nem igénylő diagnosztikai eljárás, amely még jóval a szervi elváltozások kialakulása előtt képes felismerni és helyileg behatárolni a rák kialakulásához vezető kóros folyamatokat. A vizsgálatok alkalmával túlnyomó részben egy speciális szénhidrátot juttatnak a testbe. Ez a radioaktív fluor-18 izotópot tartalmazó glükózmolekula (FDG), ami egy steril intravénás injekció hatóanyagaként kerül a szervezetbe, ahol közel 20 perc leforgása alatt a nagy energiaigényű tumoros sejtekben halmozódik fel. A PET/CT-készülék detektorai érzékelik a pozitront kibocsátó izotóp szervi megoszlását és akár 3 mm kiterjedésű aktív régiókat képes kimutatni a testben.
Becslések szerint a világon elvégzett PET/CT-vizsgálatok száma 2012-ben eléri a 4,4 milliót, ami Magyarországot tekintve meghaladja a tízezret. Figyelemre méltó történelmi érdekesség, hogy 1994-ben Közép-Kelet-Európában elsőként a Debreceni Egyetemen állítottak elő FDG-t PET-vizsgálatok céljára. Ennek a területnek a fejlődése azóta is töretlen. Jelenleg a Nukleáris Medicina Intézet Debrecenben évente 12 000 betegadagnak megfelelő dózisú FDG-t állít elő a helyes gyógyszergyártási gyakorlat szigorú irányelveit követve, amivel mind a belföldi, mind a környező országok radiogyógyszer-igényeit maradéktalanul kielégíti.
Kényes egyensúly
Az FDG a gyógyszerek speciális képviselője, mivel a készítmény milliliterenként átlagosan mindössze 10 mikrogramm hatóanyagot tartalmaz, ami ráadásul az idő előrehaladtával folyamatosan csökken a fluor-18 izotóp rövid, 110 perc felezési idejének köszönhetően. Ez azt jelenti, hogy a hatóanyag mennyisége a gyógyszerkészítményben a gyors spontán radioaktív bomlás miatt alig 2 óra alatt a felére csökken, és a folyamat nem áll meg. Átlagosan 10-12 óra alatt fel kell használni a készítményt, máskülönben csak sóoldat marad utána. Ez azt jelenti, hogy a PET-vizsgálatokhoz naponta új gyártási tételt kell előállítani, ami az izotóptermeléssel kezdődik a ciklotronban, majd – az emberre káros sugárhatás kivédése végett – zárt ólomfülkében elhelyezett automata szintézisberendezésen történik az izotóp beépítése a glükózmolekulába. A folyamat az injekció ampullába töltésével és a minőség ellenőrzésével zárul.
A növekvő tendenciát mutató PET/CT-vizsgálatok és az FDG-előállítás költséghatékony kivitelezése azt az elvárást támasztja a gyógyszergyártás elé, hogy egy gyártási tétel a lehető legnagyobb radioaktivitást tartalmazza. Ez az FDG esetében – mint a legtöbb radiogyógyszernél – speciális problémát vet fel: ez pedig a radiolízis. „Radio” azt jelenti, sugárzás, a lízis pedig bomlás. Azaz a hatóanyag-tartalom növekedésével nő a készítmény radioaktivitása, ami fokozza az olyan reaktív részecskék termelődését, mint a szabadgyökök, amelyek a vízmolekulák felhasadásával képződnek a megnövekedő sugárdózis hatására. A hihetetlenül reakcióképes részecskék végeredményben megtámadják magát a hatóanyag-molekulákat, amelyek ennek hatására felbomlanak. Tehát a gyógyszermolekulákat saját radioaktív izotópjuk veszélyezteti. A folyamat következményeként nemcsak csökken a hatóanyag-tartalom, de a gyógyszermolekula felhasadása során radioaktív fluor-18-ion keletkezik, amely radiokémiai szennyezőnek tekinthető, vagyis csökken a készítmény tisztasága. A gyógyszergyártási követelmények szigorúan megszabják, hogy a készítmény radioaktív komponenseinek legalább 95%-a FDG kell legyen. Ellenkező esetben a magas fluor-18 szint a PET/CT-vizsgálatok során kritikus következményekhez vezethet: a helyes diagnózist meghiúsíthatja a csontozatban dúsuló fluor-18 ion, amivel a kis kiterjedésű rosszindulatú gócok nehezen vagy egyáltalán nem észrevehetőek. Tehát a hatóanyag kémiai értelemben vett stabilitásának biztosítása nagy radioaktivitású készítményekesetében kritikus.
Mi roncsol?
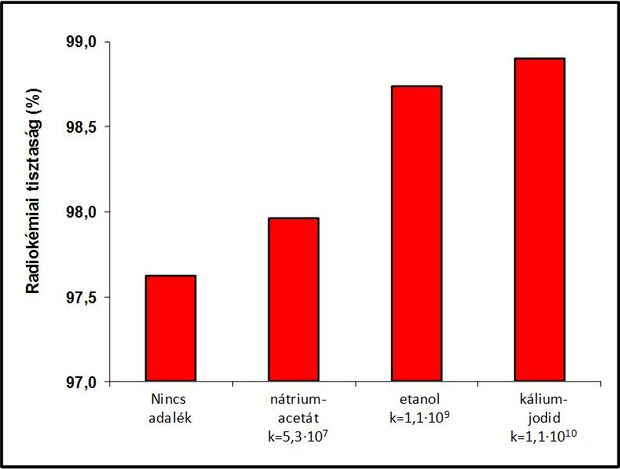
Az FDG radiolízisének visszaszorítása érdekében a kutatók általában valamilyen redukálószert adnak a gyógyszerhez (pl. aszkorbinsavat), amely megköti és semlegesíti a reaktív részecskéket, ezzel megvédve a hatóanyag molekuláit. Az adalékanyagok akár ezerszer nagyobb mennyiségben lehetnek jelen a készítményben, mint maga az FDG. Ez egyben azt is jelenti, hogy a segédanyag találkozásának valószínűsége a reaktív részecskékkel sokkal nagyobb. Ez az egyik ok, amiért ezek a vegyületek stabilizáló hatást fejtenek ki. Ugyanakkor eddig nem volt ismert egy jól meghatározott szabály, amely alapján ki lehet választani a hatékony stabilizátorokat. A Debreceni Egyetem Nukleáris Medicina Intézetében több éves kutatómunka eredményeként sikerült orvosolni ezt a hiányosságot. Ismereteink alapján a radioaktív sugárzás hatására a vízmolekula felbomlása két olyan reaktív részecskét eredményez, amely az FDG-t kiemelten veszélyezteti. Ez a hidroxilgyök (OH•), amely erős oxidálószer, és a hidratált elektron, ami kiszorítja a fluor-18 atomot a hatóanyagmolekulából. Kísérleteinkkel eldöntöttük, hogy közülük a hidroxilgyök sokkal aktívabban lép kölcsönhatásba az FDG-vel, így nagyobb veszélyt jelent a hatóanyag stabilitására. A következtetésre úgy jutottunk, hogy ugyanazon radioaktív készítmény egy-egy mintájához két különböző sóvegyületet adtunk egyforma mennyiségben. Az egyik esetben ammónium-formiátot használtunk, amely nagyságrendekkel gyorsabban reagál a hidroxilgyökökkel, mint a hidratált elektronokkal. Ez a vegyület szelektív hidroxilgyök-befogónak tekinthető. A második esetben pedig kálium-nitrátot adtunk a mintához, ami szelektíven semlegesíti a hidratált elektronokat. Az így kezelt gyógyszermintákat négy órával a stabilizátorok hozzáadását követően vékonyréteg-kromatográfiás módszerrel megvizsgáltuk, amely segítségével képesek voltunk elkülöníteni az FDG-molekulákat, valamint a fluor-18 ionokat és meghatározni a hatóanyag részarányát. Az ammónium-formiátot tartalmazó minta radiokémiai tisztasága a kiindulási 98,5%-ról 96,8%‑ra csökkent. A kálium-nitráttal kezelt minta esetében ez az érték már 95,4%-nak bizonyult. Az ammónium-formiátot tartalmazó minta tisztaságának kisebb mértékű csökkenése arra enged következtetni, hogy a szelektív hidroxilgyökfogó tulajdonságú vegyületeket érdemes választani az FDG stabilizálására, mivel ezek a hatóanyag molekulát nagyobb mértékben veszélyeztető OH•-részecskét nagy hatékonysággal semlegesítik. Az is kiderült, hogy a szelektív hidroxilgyökfogó vegyületek stabilizáló hatás tekintetében eltérhetnek egymástól, amit a stabilizátorok és a hidroxilgyök között lejátszódó folyamat sebessége határoz meg. A reakció gyorsaságának mértékéről az úgynevezett sebességi állandó (k) ad felvilágosítást, ami megadja az egységnyi idő alatt átalakult molekulák számát. Minél nagyobb egy folyamat sebességi állandója, annál gyorsabban megy végbe. Esetünkben ez azt jelenti, hogy annál hatékonyabb stabilizáló hatásról beszélhetünk. Ezt alátámasztják az eltérő sebességi állandóval rendelkező hidroxilgyökfogó vegyületekkel végzett kísérletek eredményei, mivel a legnagyobb k-értékkel rendelkező kálium-jodid hatására a készítmény radiokémiai tisztasága tekintetében a legkisebb csökkenést tapasztaltuk.
Vitamin és gyümölcscukor?
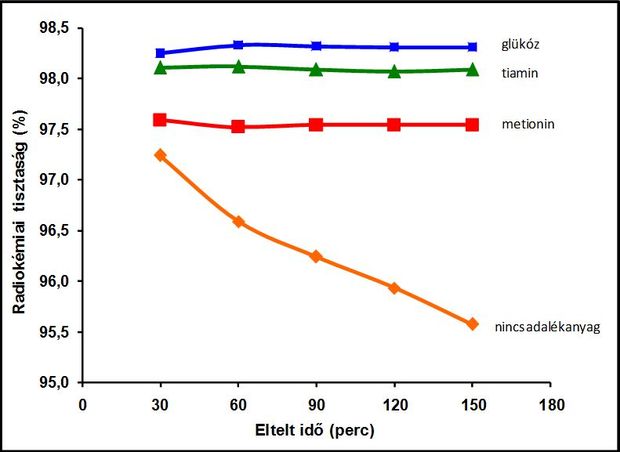
Szabályként kimondható tehát, hogy az FDG radiogyógyszer stabilitása és egyben tisztaságának megőrzése végett olyan vegyületet érdemes a készítménybe segédanyagként juttatni, amely szelektív hidroxilgyökfogó tulajdonsággal rendelkezik és az hidroxilgyökkel adott kölcsönhatás sebességi állandója a lehető legmagasabb. Ezt az irányelvet követve olyan kémiai komponensek javasolhatók hatékony stabilizátoroknak, amelyek nem feltétlenül redukálószerek, mint ahogyan a szakirodalom ajánlja, és egyben teljes mértékben kielégítik a velük szemben támasztott elvárásokat a készítmény radiokémiai tisztaságának megőrzése tekintetében. Továbbá alapvetően fontos kitétel, hogy a segédanyagok ne jelentsenek egészségügyi kockázatot a betegekre, azaz ne legyenek mérgezőek. Ezt a szempontrendszert figyelembe véve az FDG stabilizálására három kémiailag különböző családba tartozó vegyületet ajánlunk. Ezek a metionin (természetes aminosav), a glükóz (gyümölcscukor) és a tiamin (B1-vitamin). Ezek a stabilizátor-jelöltek valóban szelektív hidroxilgyökfogók, nagy k-értékkel rendelkeznek és mindemellett nemhogy károsak, de jótékony hatásúak az emberi szervezetre. Ezen vegyületek FDG-re gyakorolt stabilizáló hatását külön-külön behatóan tanulmányoztuk. Arra a következtetésre jutottunk, ha az említett vegyületek már 1%-ban jelen vannak az injekciós készítményben, akkor kitűnően alkalmazhatók a hatóanyagmolekulák megvédésére. Ezt arra alapozzuk, hogy az egyes stabilizátorral kezelt FDG-minták radiokémiai tisztasága csaknem állandó maradt több órán át, miközben az adalékanyagot nem tartalmazó minta minősége jelentősen romlott és majdnem elérte a kritikus 95%-os szintet.
A radioaktív FDG-gyógyszermolekula stabilizálására irányuló kutatási eredmények birtokában egy új PET-létesítmény telepítésekor a radiogyógyszergyártás úgy tervezhető vagy a már üzemben lévő technológia úgy módosítható, hogy a nagy radioaktivitású készítmények jó hatásfokkal és biztonsággal megőrizzék radiokémiai tisztaságukat egészen a gyógyszer eltarthatósági idejének végéig.
JÓSZAI ISTVÁN
2014/6





